
患者:男性,66岁。
患者诉10月前无明显诱因开始出现间胸闷、气喘,活动后加重,偶有咳嗽、咳白痰,无咯血、胸痛,无畏寒、发热,无腹痛、腹胀、腹泻,4月前胸闷、气喘稍加重,未重视,一直未就医,10余天前出现胸闷加重,遂至当地医院就诊,行胸片示:双肺多发感染,予以抗感染等治疗,未见好转,昨日至我院就诊
两肺弥漫分布磨玻璃影,并见小叶间隔及小叶内间质增厚,呈明显铺路石征,病变与正常肺边界清晰,呈地图样改变,其内见支气管充气征,左下肺部分支气管稍扩张,冠状位重建示病变以中下肺野为主,胸膜下分布较少累及,心影不大,纵隔内见多发稍大淋巴结影,未见明显胸腔积液。影像诊断:考虑PAP
肺泡蛋白沉积症(PAP)
已行手术:大容量左肺灌洗术
手术过程:麻醉成功后,患者取仰卧位,经口插入型号32号双腔气管导管,可视确认导管位置,隔离目标肺与健侧肺。连接灌洗装置,准备37℃无菌生理盐水12 L(根据患者情况调整),经加温装置预热。向目标肺缓慢注入37℃生理盐水1000ml,轻拍胸壁促进肺泡内蛋白样物质排出,停留数秒后,通过负压吸引装置回收灌洗液。重复上述灌洗-吸引步骤12次,直至回收液由浑浊逐渐变澄清,吸尽残留灌洗液,恢复自主呼吸,血压、血氧稳定后拔除双腔气管导管,听诊双肺呼吸音粗糙,观察有无出血、气胸、肺水肿等并发症。灌洗总量:11L,回收液总量:10.9L,回收率约99%。回收液性状:初始为乳白色浑浊液体,含大量胶冻样或泥沙样物质;终末回收液接近澄清。患者生命体征平稳,术中未出现低氧血症、血压骤降等严重并发症。

肺泡蛋白沉积症(pulmonary alveolar proteinosis,PAP)是一种由肺泡表面活性物质代谢异常引起表面活性蛋白和脂质沉积于肺泡内,进而 导致肺通气和换气功能障碍的肺部罕见病,发病率仅为 0.36~3.70/100 万。PAP 十分罕见,起病隐匿,且临床表现缺乏特异性,故常被误诊为反复发作的肺炎 、哮喘 、肺气肿等 ,延误最佳诊疗时机 。
PAP是一种罕见的肺部弥漫性疾病,以肺泡巨噬细胞功能障碍及肺泡表面活性物质在肺泡腔内积聚为特征,病理表现为肺泡腔内堆积过碘酸-希夫(periodic acid-Schiff,PAS)染色阳性的无定型蛋白样物质,进而引起亚急性进行性呼吸功能障 碍 。根据发病机制,PAP可分为原发性(可进一步分为自身免疫性和遗传性两种亚型)、继发性和先天性3种类型:(1)原发性PAP由GM-CSF信号传导通路异常,引起巨噬细胞和粒细胞功能障碍所致,是发病率最高的PAP类型,约占90%。其中自身免疫性PAP又称特发性PAP,由自身GM-CSF抗体水平过高所致;遗传性 PAP由编码GM-CSF受体亚基的基因(CSF2RA 或 CSF2RB)突变引起。(2)继发性PAP常继发于恶性肿瘤、慢性血液系统疾病、慢性炎症和感染、免疫缺陷、有毒物质吸入或职业暴露等,约占5%。(3)先天性PAP由编码肺泡表面活性物质相关基因(SFTPB、SFTPC、 ABCA3 等)突变导致表面活性物质代谢异常引起, 多见于儿童,约占 5%。
PAP的临床与病理:PAP的发病年龄广泛,但多见于30至50岁成人,且男性患者显著高于女性。该病程通常较长,可能延续数月乃至数年,初期常无明显症状,多在体检时偶然发现。疾病进展相对缓慢,主要症状包括逐渐加重的呼吸困难、活动诱发的胸闷与气短,以及感染时的咳嗽、咳痰。部分患者还可能经历咯 血、杵状指(趾)或紫绀等体征。PAP的预后存在显著差异,少数患者可能自行缓解,但也有部分患者因呼吸衰竭而危及生命 。值得注意的是,PAP患者的临床表现与影像学所见往往不呈直接对应关系,影像学改变可能更为显著。肺功能测试是评估病情严重程度的重要手段,多数患者表现为限制性通气障碍及气体弥散能力下降,伴随通气/血流比例失衡,进而引发低氧血症。对于PAP的确诊,组织病理学检查具有决定性意义。典型的支气管肺泡灌洗液呈乳白色,而肺活检则揭示肺泡及细支气管腔内充斥大量PAS染色阳性的磷脂蛋白性颗粒物质,同时小叶间隔可能因水肿及淋巴细胞浸润而增厚。
PAP的CT表现:病变的分布多样,可为弥漫性或散在片状随机分布,对称或不对称,可跨段、跨叶,无叶段分布特点,最常累及肺基底部和后部,前部受累较少、较轻,一般不累及胸膜,“岛样”或“多岛样”散在分布多见于早期病例。“磨玻璃征”作为PAP在CT检查中的基本征象,其出现标志着肺泡腔内部分区域被蛋白性物质所占据,这一征象常与多种其他CT表现并存,共同反映了疾病的复杂性。其中,GGO(磨玻璃影)特指肺泡腔内蛋白性物质的部分充填状态。当肺泡腔内这类物质大量积聚时,CT图像上则转变为实变影。值得注意的是,磨玻璃密度影中还可能夹杂着小结节状影,而在中央区域的磨玻璃影及实变区内,常能观察到“支气管充气征”,这是气体在未被完全充填的支气管内残留所致。由于PAP的病变过程以肺小叶为单位进行,蛋白性物质的沉积受到小叶间隔的自然屏障作用,使得病变区域的边界相对清晰。同时,周围未受影响的肺泡腔因代偿性过度充气而显得密度降低,这种对比效应进一步增强了病变边界的清晰度,形成了所谓的“地图征”。病变内部由于小叶间隔和小叶内间质增厚形成多边形或不规则形的网格状阴影改变,与病变的GGO共同形成“铺路石征”。“地图征”和“铺路石征”在PAP的CT诊断中具有一定特征性,同时出现强烈提示本病。在特定情况下,PAP的影像学表现可能呈现出自肺门向外放射状的中央性分布模式,这种形态与肺泡型肺水肿的“蝶翼征”在视觉上有所相似,然而,关键在于PAP患者并不伴随心功能不全的其他影像学特征及临床体征,从而可将两者区分开来。
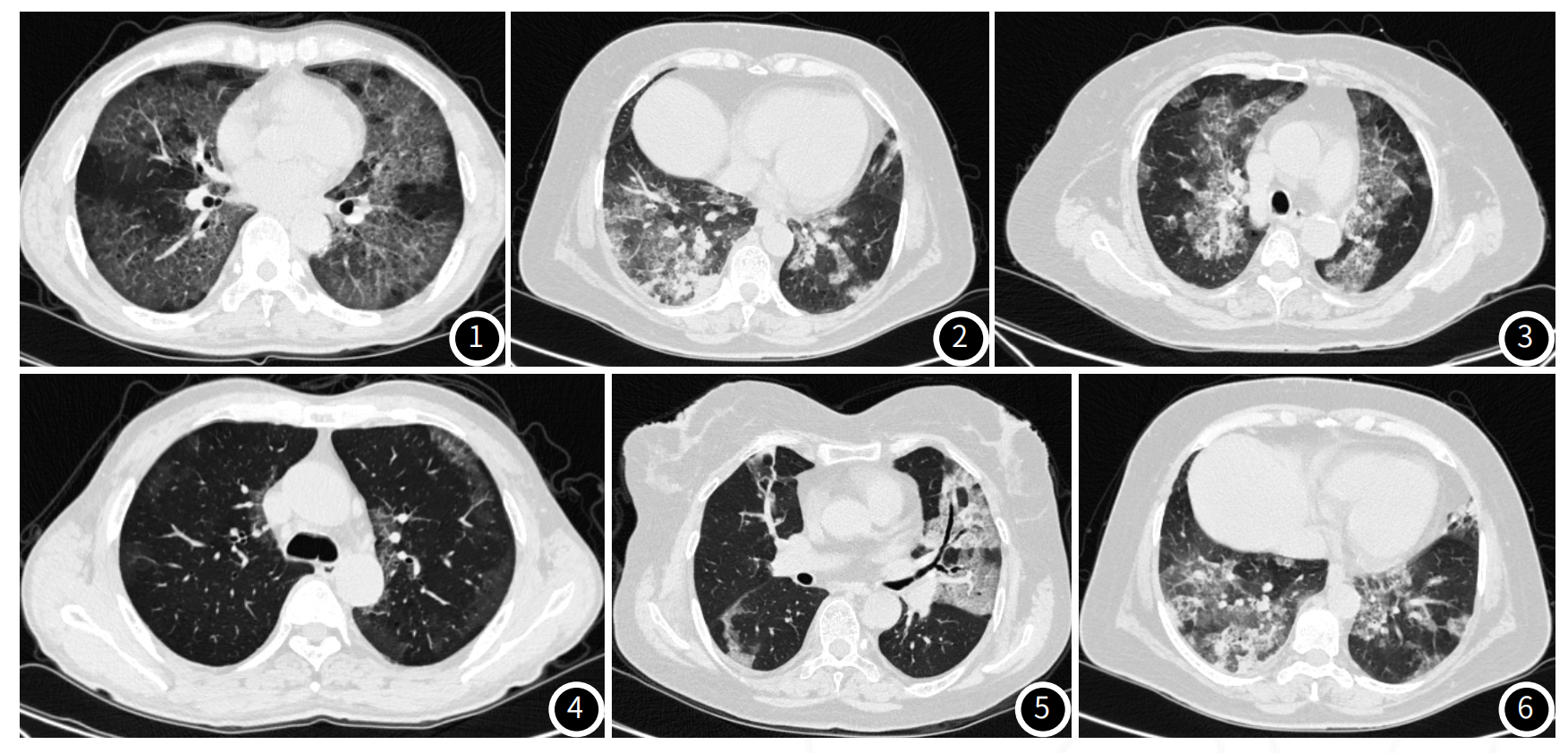
图1 双肺弥漫分布磨玻璃密度影;图2 磨玻璃密度影伴斑片状实变;图3 病变主要以肺门为中心“蝶翼状”分布, 磨玻璃密度影内见小叶间隔增厚,呈“铺路石征”;图4 病变主要分布于两肺胸膜下;图5 病变与周围正常肺组织分界清楚,边界清晰锐利,呈“地图征”改变,内可见“支气管充气征”;图6 磨玻璃密度影中见小结节状影。
鉴别诊断: ①特发性肺间质纤维化: 与PAP难鉴别,但此病主要是肺间质性小结节、GGO,与周围肺组织分界不清,小叶间隔增厚明显,可见胸膜下线,激素治疗效果好; ②肺水肿: 肺水肿容易与中央型PAP混淆,肺水肿一般合并心影增大、胸腔积液; 且肺内病灶短期内变化较快; ③肺炎: 患者症状体征较重,如发热、咳嗽咳痰,白细胞明显增高等,临床症状与影像学表现基本一致,肺内阴影边界模糊不清,可呈段叶分布,抗生素治疗有效; ④肺泡型肺泡癌: 双肺弥漫结节影、斑片影,边界不清,若出现空气支气管征则为枯枝状,常合并纵隔、肺门淋巴结明显肿大; 进展快。
邱立军, 乔宏伟, 姜敏敏. 肺泡蛋白沉积症的CT诊断分析[J]. 中国CT和MRI杂志, 2024, 22(8):45-46.
剧素贞, 王祥, 赵开顺等. 肺泡灌洗液外观不典型肺泡蛋白沉积症1例报告并文献复习[J]. 复旦学报(医学版), 2025, 52(1):147-152.
刘国芳, 张健, 龚明福等. 肺泡蛋白沉积症的高分辨CT诊断分析[J]. 中华肺部疾病杂志(电子版), 2018, 11(5):555-558.
类型:原创
病例ID:ZYLM000008113
校对:杨卢粉
阅读:458
文章已于2025-06-16修改






