
患者:男,37岁。
病史:患者约于20余年前无明显诱因出现发作性四肢强直性抽动,伴仰头、双眼上翻及间断肢体活动不灵,伴流涎、龇牙咧嘴,无进食呛咳,无肢体麻木无力,无头痛、头晕,曾多次在武汉同济医院就诊,检查提示K-F环(+),血铜低,诊断为肝豆状核变性,长期服用青霉胺、加巴喷丁、维生素B6,症状逐渐有好转;现间断出现肢体活动不灵,今为求诊治,前来我院就诊,门诊以“肝豆状核变性”收入我科。病程中曾有肝功能异常,长期服用肌苷片。患病后精神状态一般,饮食、睡眠一般,大小便正常,体力下降。
辅助检查:门诊查血清铜蛋白测定95.8mg/L↓。
颅脑MR平扫:双侧桥臂、右侧小脑半球、延髓、桥脑、中脑、双侧豆状核、壳核可见多发斑片状稍长T1、T2信号,边界不清,病灶于T2FLAIR呈高信号,大致呈对称性分布。脑室系统轻度扩大,脑沟、脑裂增宽,中脑、小脑体积缩小,中线结构未见移位。
颅脑MRA:双侧大脑前动脉、大脑中动脉、大脑后动脉主干及分支走行通畅,管壁光整,血管腔未见明显狭窄及异常扩张,未见畸形血管;双侧椎动脉、基底动脉及双侧颈内动脉颅内段通畅,管壁光整,管腔未见狭窄及异常扩张。
影像学诊断:1. 双侧桥臂、右侧小脑半球、脑干及基底核团多发异常信号伴脑萎缩改变,符合肝豆状核变性颅脑表现;2. 颅脑MRA未见明显异常。
肝豆状核变性
肝豆状核变性是常染色体隐性遗传的铜代谢缺陷病,是儿科常见的遗传代谢性疾病之一。该病于1912年由Wilson最早描述,故又称Wilson病(Wilson's disease)。本病常见于儿童和青少年,年龄范围为5~35岁。临床上以不同程度的肝损害、脑实质损害和眼角膜边缘铜盐沉着环(K-F环)、肾脏损伤、急性血管内溶血及骨关节病为主要特征。
发病机制:人体内铜主要以口服的方式从食物中吸收,在肠道吸收入血的铜绝大部分通过肝细胞的P型ATP酶,转运至胆管随着胆汁排出;少部分通过肝细胞高尔基表面的P型ATP酶,转运至高尔基体并与铜蓝蛋白的前体合成铜蓝蛋白,进入血液和组织液,血清中的铜绝大多数以铜蓝蛋白形式存在(>90%),少量与血清蛋白结合,极少量以游离铜离子形式存在。Wilson病致病基因ATP7B基因突变导致其编码的铜转运P型ATP酶功能减弱或消失,继而导致铜蓝蛋白合成减少及胆道排铜障碍,血铜总量减少,但游离铜离子含量增加,过量的游离铜离子沉积在组织器官中,可累及肝脏、神经系统、肾脏、血液系统及骨关节等器官系统,出现相应的临床症状和体征。
临床表现
1. 神经系统症状:通常为锥体外系神经症状,包括震颤、不自主运动、共济失调、肌张力障碍、肢体僵硬、运动迟缓、流涎、构音障碍、假性球麻痹、自主神经功能异常、偏头痛及癫痫等;精神症状常可早于神经症状和肝脏损害,包括躁狂、抑郁、精神分裂、神经质行为、失眠及人格改变等。
2. 肝脏损害表现:包括脂肪肝、急慢性肝炎、溶血性黄疸、肝硬化及肝衰竭。
3. 其他表现:角膜K-F环、向日葵样白内障、皮肤黝黑、溶血性贫血、氨基酸尿、肾结石、骨关节病、甲状旁腺功能减退、月经失调、不孕及心肌病等。
辅助检查
1. 角膜K-F环:在手电筒侧光照射下,肉眼可见患者角膜边缘的黄绿色或黄灰色色素环。
2. 铜代谢相关生化检查:(1)血清铜蓝蛋白<80 mg/L为Wilson病的诊断证据,铜蓝蛋白<120 mg/L应引起高度重视,需进行ATP7B基因检测明确诊断;(2)24h尿铜≥100 μg;(3)肝铜量>250μg/g。
3. 血尿常规:肝硬化伴脾功能亢进时,血常规可出现血小板、白细胞和(或)红细胞减少;尿常规可见镜下血尿、微量蛋白尿等。
4. 肝脾检查:(1)肝功能:血清转氨酶、胆红素升高和(或)白蛋白降低;(2)早期为脂肪肝、肝炎,后期为肝硬化改变,部分患者表现脾大、脾亢。
诊断标准:1. 神经和(或)精神症状;2. 原因不明的肝脏损害;3. 血清铜蓝蛋白降低和(或)24h尿铜升高;4. 角膜K-F环阳性;5. 经家系共分离及基因变异致病性分析确定:患者的2条染色体均携带ATP7B基因致病变异。符合(1或2)+(3和4)或(1或2)+5时均可确诊Wilson病;符合3+4或5但无明显临床症状时则诊断为Wilson病症状前个体;符合前3条中的任何2条,诊断为“可能为Wilson病”,需进一步追踪观察,建议进行ATP7B基因检测,以明确诊断。
Wilson病的脑部MR表现与病理机理:
最常见的影像表现为T2WI和T2-FLAIR图像上双侧壳核(70%)、尾状核(60%)、丘脑腹外侧(55%~60%)和中脑(50%)出现对称性高信号,这些区域反映了该病铜沉积的选择易损性特征;有时也可见脑桥(20%)、延髓(10%~15%)和小脑(10%)高信号,大脑白质(25%)和小脑白质(10%)可见局灶性或弥漫性融合状高信号。其机理主要是铜沉积于脑组织中,造成反应性水肿、神经元及胶质细胞缺失、海绵样变性和胶质增生,进而引起不可逆性的空腔和囊变。在未经治疗或治疗效果不佳时,随病程的延长,铜沉积逐渐增多,由于铜顺磁性作用,最终可形成T2WI低信号。T1WI图像上病变信号强度多样,部分病例的受累区表现为低信号,而部分病例则表现为高信号,类似慢性肝性脑病,反映了铜的顺磁性效应。对称性基底节异常信号同时伴有脑干病灶是该病的影像特征。当病变发展到一定程度时,随着神经元及胶质细胞广泛坏死、变性,常出现基底核团及脑干萎缩表现,甚至可出现全脑萎缩。
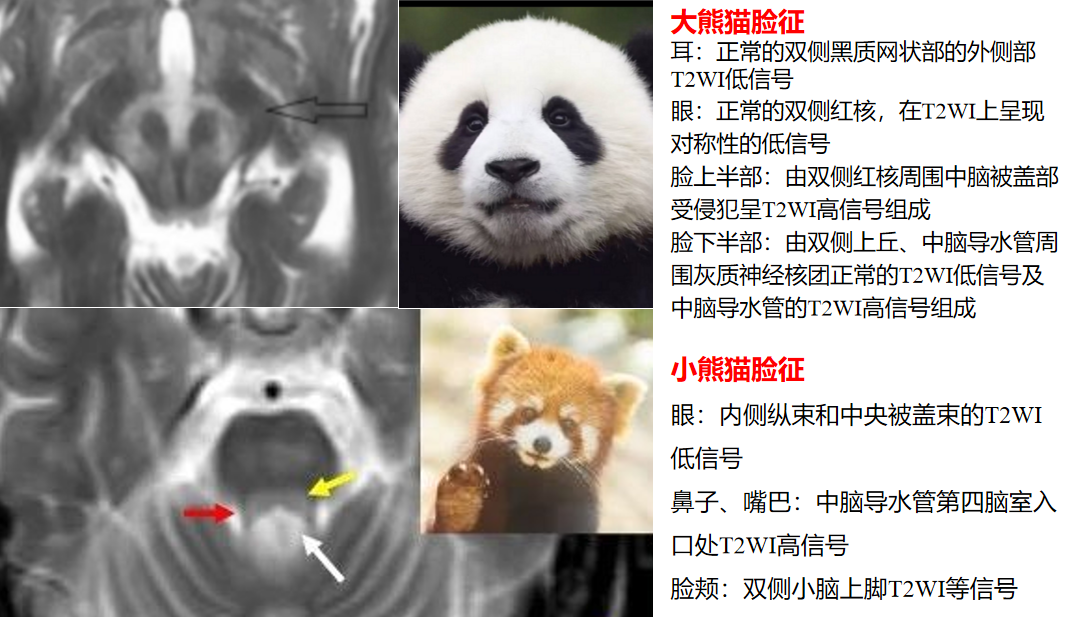
“熊猫脸征”常见于Wilson病,分为“大熊猫脸征”和“小熊猫脸征”,是该病在脑干结构选择易损性的影像学表现。T2WI图像上“大熊猫脸征”出现在中脑层面,红核为对称性低信号,构成熊猫的眼睛,而红核以外的中脑顶盖结构高信号构成熊猫的上半身白色轮廓,侧面的黑质网状部的正常信号构成耳朵,上丘低信号构成嘴巴。“小熊猫脸征”出现在脑桥被盖层面,内侧纵束和中央被盖束呈低信号构成小熊猫眼睛,导水管开口进入第四脑室的高信号构成鼻子和嘴。需要注意的是“熊猫脸征”并非Wilson病脑部MRI特征性表现,其他疾病如Leigh病、脑干梗死、EB病毒相关性脑炎、甲硝唑脑病、甲醇中毒及缺血缺氧性脑病等也可出现该征象。
鉴别诊断:主要包括其他累及基底节的遗传性代谢性疾病,如Leigh综合征,脑铁质沉积性神经变性等。Leigh综合征即亚急性坏死性脑脊髓炎,表现为双侧壳核和脑干的对称性高信号,病变常累及白质,很少累及尾状核和丘脑,MRS可见基底节乳酸峰升高。泛酸激酶相关性神经变性(PKAN)的表现也可类似于Wilson病,但Wilson病主要累及壳核和尾状核,而非苍白球内侧,且无PKAN的特性性“虎眼”征。
治疗与预后:Wilson病的治疗应遵循“早期治疗,终身治疗,终身监测”原则,具体治疗包括个体化应用排铜或阻止铜吸收的药物和锌制剂、对症治疗、手术治疗、终身低铜饮食及动态监测治疗效果和药物不良反应。经过长期规范的排铜治疗或肝移植治疗,Wilson病患者的寿命可大幅延长,尤其是在疾病早期,神经症状出现之前进行干预,大部分患者可回归正常的工作和生活。该病主要死于严重的肝脏疾病或严重的神经症状,少数患者因疾病负担或抑郁自杀。
类型:原创
病例ID:ZYLM000007832
校对:李文文
阅读:814
文章已于2025-05-26修改






