男,67岁,反复走路不稳、双手抖动半年入院
既往:体健
体格检查:双手震颤、肌强直、行走缓慢,类似帕金森样症状。
实验室检查:无特殊。
案例分析
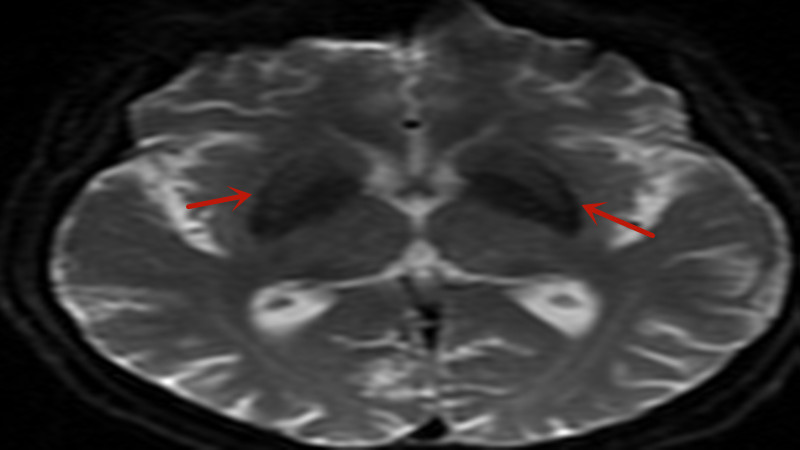
MRI表现:小脑萎缩,DWI示双侧壳核见裂隙状低信号(尤其B=0较明显),提示异常金属离子沉积。
临床诊断:多系统萎缩(MSA-P型)可能。
多系统萎缩(MSA):是一组成年期发病、散发的自主神经功能障碍的神经变性疾病,临床表现为进行性小脑性共济失调、 自主神经功能不全和帕金森综合征等症状,病因和发病机制未明。
发病机制:目前认为可能有两条途径:
1、原发性少突胶质细胞病变假说,即先出现以α-突触核蛋白(a-
synuclein)阳性包涵体为特征的少突胶质细胞变性,导致神经元髓鞘变性脱失,激活小胶质细胞,诱发氧化应激,进而导致神经元变性死亡;
2、神经元本身a-突触核蛋白异常聚集,造成神经元变性死亡。a-突触共核蛋白异常聚集的原因尚未明确,可能与遗传易感性和环境因素有关。
流行病学:好发于中老年人,散发、无明显家族遗传学。
临床分型:MSA-P和 MSA-C型
病理:少突胶质细胞α-突触蛋白病
形态学改变:桥脑、桥壳、桥脑基底部、小脑中脚、小脑半球萎缩等
MSA-P型影像学表现和病理改变:
1)壳核萎缩: 壳核变小、厚度变薄,壳核弧度消失、变直(机制:神经元丢失及胶质纤维增生)
2)壳核裂隙征: 壳核外侧边缘T2WI高信号环(机制:壳核外侧神经元缺失以及胶质增生,壳核萎缩引起组织间空隙增大产生的)(壳核裂隙征于3.0TFlair序列及1.5TT2WI序列敏感,高磁场如3.TMRI正常人有可能出现T2WI裂隙征)
3)壳核T2WI/DWI/SWI低信号:壳核背外侧可见等于或低于苍白球信号的异常信号(机制:铁蛋白丢失、铁沉积引起)。
MSA-C型影像学表现和病例改变
1) 脑桥、小脑和延髓橄榄核的萎缩
2)“脑桥十字征”:T2WI序列脑桥层面上“十字形”高信号带
(机制:脑桥核及发出的通过小脑中脚到达小脑的纤维(桥横纤维)脱髓鞘、胶质细胞增生,而齿状核发出的构成小脑上脚的纤维和锥体束未受累所致。有学者认为,先出现“垂线征”,后出现“十字征”。“十字征”形成过程与桥脑小脑萎缩程度之间存在相关性,当“十字征”越明显,对应其桥脑面积越小)
3) 伴随征象:四叠体池、桥前池、桥小脑角池及小脑延髓池增大,四脑室也扩大
鉴别诊断:
1)进行性核上性麻痹(PSP):属于神经变性疾病,tau蛋白,表现为中脑、基底节、额叶皮层、中脑、小脑上脚萎缩,MRI典型征象:蜂鸟征、牵牛花征。
2)帕金森病(PD): 由于铁代谢异常,过多的铁沉积在黑质致密部(后1/3)引起氧化过激等多种反应,导致中脑黑质多巴胺(DA)能神经元的变性死亡(进行性缺失),由此而引起黑质-纹状体DA含量显著性减少而致病。薄层高分辨SWI显示正常的黑质小体-1高信号消失,即燕尾征消失(单侧或双侧出现), 也有研究者发现PD可伴有基底节区-桥壳的异常金属离子的沉积而出现SWI信号减低,但PD不及MSA-P型异常金属离子沉积明显。
治疗:MSA在治疗方面尚无有效治疗方法,主要以对症治疗和神经保护治疗为主,对于MSA-P型患者还是考虑加用多巴胺能药物以控制症状。
类型:原创
病例ID:ZYLM000003907
校对:王宇军
阅读:1326
文章已于2023-12-18修改






