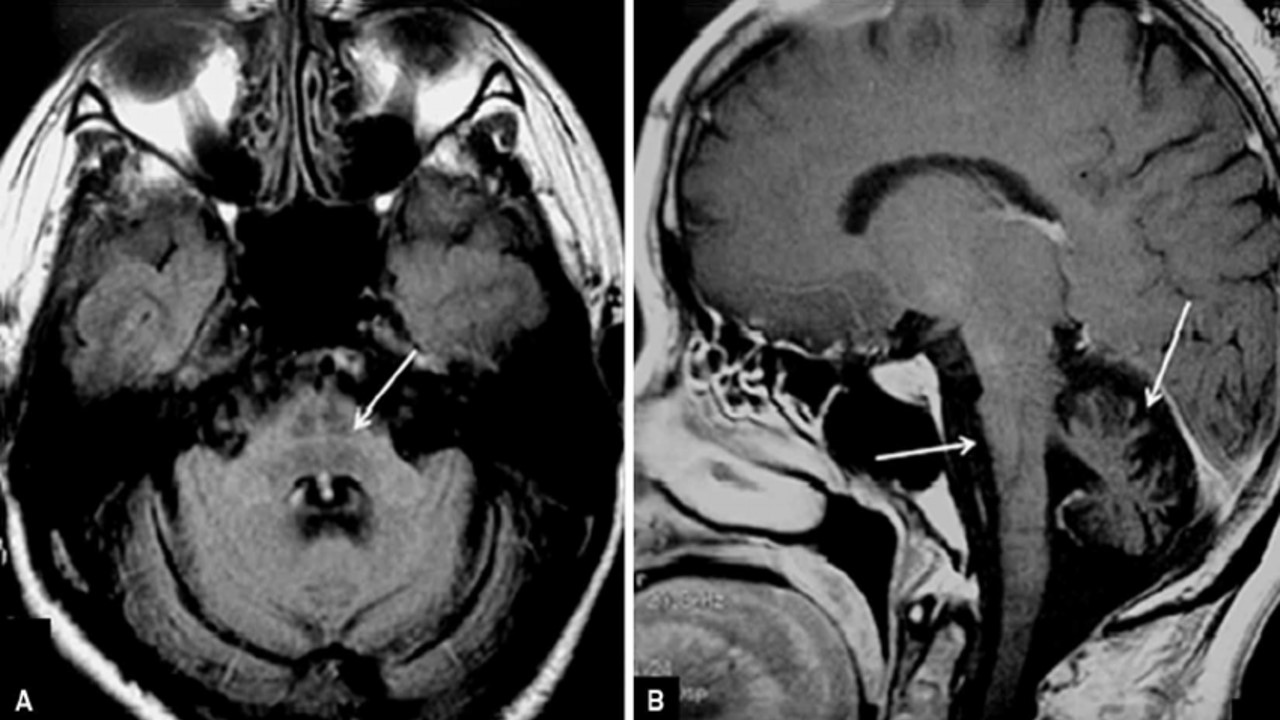
女,71岁,行走不稳伴头晕3年余,加重伴胸闷1年。
现病史
患者3年余前无明显诱因出现阵发性头晕伴行走不稳,乏力感,遂来我院住院就诊,当时考虑多系统萎缩,予营养神经等治疗后出院。2年余前感症状加重,伴言语不清,又至我院就诊,予尼可林、叶酸、维生素B6等治疗后头晕好转后出院。1年来,患者自感行走不稳、言语不清逐渐加重,伴胸闷不适,再次于我院住院治疗。
病来,患者神清,精神尚可,胃纳一般,大小便不能自控,夜寐可,近来体重增减情况不详。
病案讨论
1、小脑、脑桥形态较小,并可见“十字面包征。
2、桥前池、环池、四叠体池及第四脑室扩大
3、双侧小脑半球脑沟增宽、加深
4、临床病史:行走不稳伴头晕3年余,言语不清2年。
诊断:多系统萎缩(MSA-C型)。
多系统萎缩(MSA)是一种成年起病的进展性神经退行性疾病,其病因不明,临床主要表现为自主神经功能障碍、帕金森综合征和小脑综合征等多种组合,早期诊断相对困难,预后不佳。为了更好地规范我国临床医师对MSA的诊断和鉴别,多位专家结合我国临床实际,对我国MSA诊断标准专家共识进行内容上的更新,以期提高临床医师对MSA诊断的正确率,减少漏诊与误诊。
临床表现
MSA临床表现为自主神经功能障碍、帕金森综合征和小脑综合征的多种组合。MSA根据首发运动症状和(或)运动症状严重程度分为MSA-P型和MSA-C型,以帕金森综合征为主的患者为MSA-P型,以小脑综合征为主的患者为MSA-C型。早期出现进展性的严重自主神经功能障碍是MSA的主要特征,并影响患者的生存期。MSA常见的死因包括呼吸道感染和猝死。
1.核心临床表现(图1B)
(1)帕金森综合征:MSA-P型以帕金森综合征为突出表现,主要表现为运动迟缓,伴肌强直或震颤,但帕金森病典型的“搓丸样”震颤少见,多为皮质震颤。MSA患者帕金森综合征进展快,容易出现姿势平衡障碍,往往对多巴胺能药物应答欠佳。帕金森综合征与患者黑质纹状体变性有关。
(2)小脑综合征:临床表现为步态共济失调、肢体共济失调、小脑性构音障碍和小脑性眼动障碍(持续凝视诱发的水平型或下跳型眼震和扫视性眼动过度),与橄榄脑桥小脑萎缩有关。
(3)泌尿系统功能障碍:临床表现包括储尿和排尿功能异常,前者表现为尿频、尿急、夜尿、尿失禁,统称为膀胱过度活动征;后者包括排尿费力、尿流间断、尿线细而无力、排尿不尽感、重复排尿等。上述症状与中脑导水管周围灰质腹外侧区和脑桥排尿中枢处的神经元损伤有关(多致储尿功能异常)以及骶髓副交感节前神经元和骶髓前角Onuf运动神经核团的丢失有关(多致排尿功能异常)。急迫性尿失禁指在没有泌尿系统感染的情况下,MSA患者可突然出现较急的尿意伴不自主漏尿,这两种症状可用于鉴别诊断MSA与帕金森病。
(4)心血管自主神经功能障碍:临床主要表现为神经源性体位性低血压(nOH),患者出现头晕、晕眩、晕厥,也可出现头颈部疼痛、乏力、恶心、思维减慢、视物模糊、直立性呼吸困难、心绞痛等,常伴发夜间或仰卧位高血压。nOH与延髓头端腹外侧兴奋性交感神经元和胸段脊髓中央外侧柱交感节前神经元退行性变有关。
2.其他非运动症状(图1B)
(1)喘鸣:患者由于声门裂狭窄在睡眠或清醒时发出高调的吸气声,夜间喘鸣不易被发现。
(2)睡眠障碍:MSA患者可见多种形式的睡眠障碍。快速眼球运动期睡眠行为障碍(RBD)是突触核蛋白病的常见症状,表现为快速眼球运动(REM)睡眠期出现梦境演绎,导致受伤或睡眠受扰。RBD的诊断要满足4个条件:①反复发作睡眠相关发声和(或)复杂动作;②异常行为经视频多导睡眠监测(vPSG)证实出现于REM睡眠期,或者基于梦境扮演病史推测异常行为出现在REM睡眠期;③vPSG提示REM睡眠期无肌张力缺失;④不能以另一种睡眠疾病、精神疾病、药物和物质应用所解释。睡眠呼吸暂停和低通气也是MSA患者常见的睡眠呼吸障碍。
(3)吸气性叹息:临床表现为不自主地深吸气叹息或喘息,常见于夜间非快速眼球运动睡眠期的N1和N2睡眠期,与脑干中前包钦格复合体神经元变性有关。
(4)冷手冷脚:表现为冷手冷脚和肤色变化(紫色或蓝色),按压可发白,恢复较慢,提示血液循环回流不佳。与肢体末端血管交感神经调控障碍有关。
(5)勃起障碍:临床表现为无法勃起或勃起维持困难导致性功能障碍。勃起障碍是MSA男性患者最常见的自主神经功能异常。
(6)强哭强笑:临床表现为患者突然出现不受控制和不合时宜的大哭或大笑,可通过询问病史了解。通常与皮质-脑桥通路受损导致情绪表达障碍有关。
(7)泌汗功能异常:MSA患者可表现出节前型无汗症和节前节后混合型无汗症,MSA患者的泌汗功能障碍较帕金森病患者更严重。
3. 其他运动症状(图1B)
(1)姿势不稳:表现为后拉试验时患者退后3步及以上,或在没有检查者帮助的情况下有跌倒的倾向。与黑质纹状体多巴胺能系统和脑桥脚间核胆碱-谷氨酸能系统退行性变有关。姿势不稳通常可见于病程1年内的PSP患者、病程3年内的MSA患者以及病程10年内的帕金森病患者。
(2)口面部肌张力障碍:表现为不自主的口面部运动异常,可由左旋多巴诱发或加重,不伴或仅伴有轻微的肢体运动障碍。可能因黑质纹状体系统退行性变导致三叉神经、面神经运动障碍。
(3)咽喉肌运动障碍:患者可出现构音障碍,表现为发音困难、说话缓慢含糊,通常需要重复对话。患者也可表现为吞咽困难、流涎,需要调整饮食进行适应。与疑核损伤有关。
(4)巴宾斯基征阳性:是上运动神经元损伤的表现,需要排除颅内肿瘤、感染、脑血管疾病、脱髓鞘疾病、代谢性疾病和脊髓型颈椎病等其他原因导致的病理征阳性。
(5)肌阵挛样姿势性或动作性震颤:当患者维持抵抗重力的姿势或自主运动时,手或手指出现不规律的小幅度震颤,伴刺激敏感的肌阵挛。
(6)姿势畸形:至少包括以下1项,颈部前屈或侧屈、躯干前屈、Pisa综合征和手足挛缩。颈部前屈或侧屈可在一定程度上通过自主或被动运动纠正,Pisa综合征表现为严重的脊柱侧屈,手足挛缩需排除掌腱膜挛缩症(Dupuytren综合征)、CBS或其他原因导致的挛缩。与早中期帕金森病患者相比,颈部前屈、躯干前屈、Pisa综合征和手足挛缩等姿势畸形更常见于MSA患者。
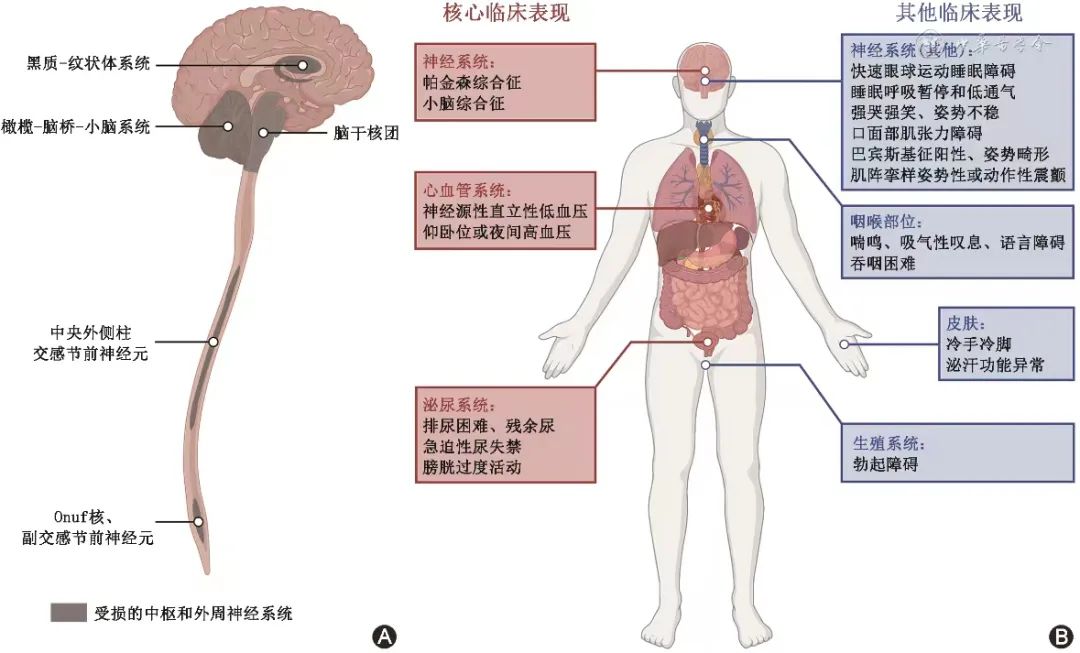
图1 多系统萎缩患者的病理与临床表现。A:多系统萎缩患者的病灶分布;B:多系统萎缩患者的临床表现
辅助检查
辅助检查根据其对临床诊断的价值分为必要性辅助检查和选择性辅助检查。必要性辅助检查对MSA诊断和鉴别诊断以及评估患者的病情有重要意义。选择性辅助检查对诊断MSA有一定的参考价值,临床医生可根据自身设备与人员条件适当完善(表1)。

1. 神经影像学检查
(1)磁共振成像(MRI):MSA患者表现为常规MRI序列上壳核、脑桥、小脑中脚和小脑萎缩,磁敏感序列上壳核的信号降低,T2序列上脑桥十字形高信号(十字征),弥散加权成像上壳核和小脑中脚弥散系数增加(图2)。MSA-C型患者通常伴有小脑萎缩的表现。由于特发或遗传的小脑萎缩性疾病也可出现小脑萎缩或小脑中脚弥散系数增加,因而小脑萎缩或小脑中脚弥散系数增加不能单独作为临床确诊MSA-C型的影像学依据(表2)。
(2)放射示踪成像:18氟-氟代脱氧葡萄糖-正电子发射体层摄影(18F-FDG-PET)显示MSA患者壳核(后侧)、脑桥和小脑处于低代谢,可用于鉴别MSA与帕金森病。多巴胺转运体-单光子发射体层摄影(DAT-SPECT)可进行突触前多巴胺能成像,MSA-C型患者DAT摄取能力下降,SAOA患者DAT摄取能力保持正常,可用于早期鉴别诊断MSA-C型和SAOA,但在鉴别诊断MSA-P型和帕金森病时证据不足。而多巴胺转运体-正电子发射体层摄影(DAT-PET)由于具备较高的分辨率,可将纹状体进行区域划分:腹侧纹状体、尾状核前部、尾状核后部、壳核前部、壳核后部和壳核腹侧部。
(3)经颅超声成像:有研究报道MSA-P型患者黑质回声多正常,黑质高回声能在一定程度上鉴别MSA-P型与帕金森病,但各项研究结果结论不一致,其鉴别诊断的敏感度与特异度欠佳。
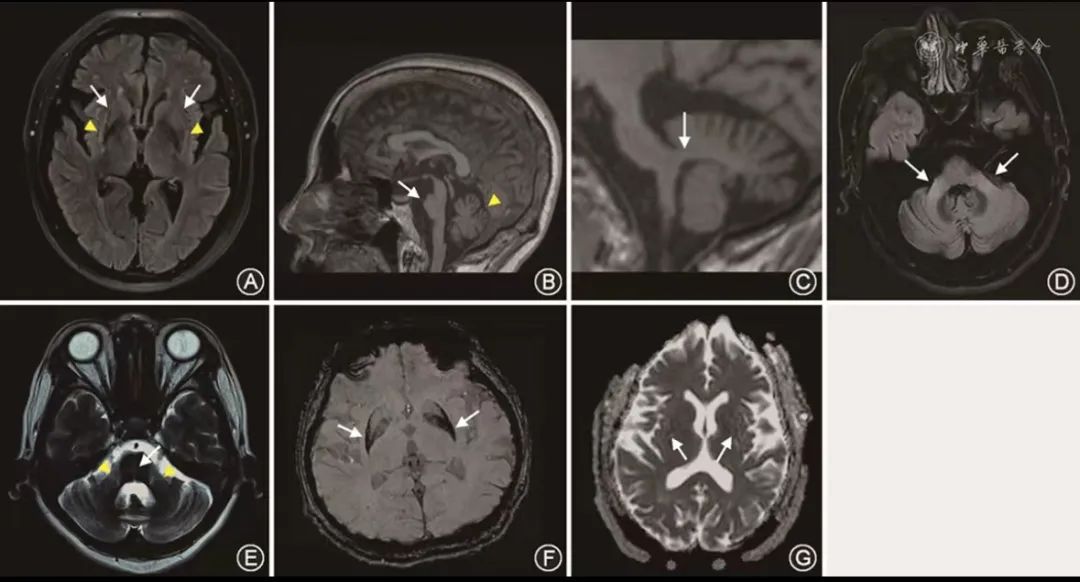
图2 多系统萎缩的磁共振成像标志物。A:T2液体衰减反转恢复序列(FLAIR)横断位上可见壳核萎缩(长箭头)和壳核背外侧缘条带状弧形高信号(三角箭头);B:T1矢状位上可见脑桥萎缩(长箭头)与小脑萎缩(三角箭头);C:T1矢状位上可见小脑中脚萎缩(箭头);D:T2 FLAIR横断位上可见小脑中脚萎缩与高信号征(箭头);E:T2横断位上可见十字征(长箭头)与小脑中脚高信号(三角箭头);F:磁敏感加权成像横断位上可见壳核尾部低信号(箭头),提示铁沉积;G:表观弥散系数成像横断位上可见壳核高信号(箭头),提示弥散系数增加(图片来源于上海交通大学医学院附属瑞金医院神经内科)

2. 自主神经功能检查
(1)泌尿系统功能评价:①残余尿:膀胱超声、尿流动力学试验可用于测量残余尿,残余尿量超过100ml是诊断临床确诊的MSA的重要指标。随着病情进展,显著的残余尿增多可用于鉴别MSA与帕金森病、SAOA,但不能鉴别MSA与PSP。②尿流动力学试验:主要监测尿流率、膀胱收缩指数、膀胱顺应性等指标。尿流率根据测量方法分为自由尿流率和压力尿流率,MSA患者的最大尿流率(Qmax)通常降低,表现为自由尿流率的Qmax<4.5ml/s,压力尿流率的Qmax<3.5ml/s。膀胱收缩指数(BCI)可准确反映膀胱的收缩功能(BCI=最大尿流率时的逼尿肌压力+5×压力尿流率试验下的最大尿流率),BCI<36.5提示MSA,可用于鉴别MSA与帕金森病。膀胱顺应性可利用膀胱容量变化与逼尿肌压力变化的比值进行计算,比值<20ml/mmH2O(1 mmH2O=0.0098kPa)称为膀胱顺应性下降,常见于MSA患者。③逼尿肌括约肌协同障碍:通过尿流动力学试验联合肌电图或膀胱尿道造影诊断,表现为排尿过程中逼尿肌的收缩伴随尿道外括约肌电活动升高,或影像上出现尿道狭窄,提示MSA。帕金森病患者不常出现逼尿肌括约肌协同障碍,但常出现逼尿肌过度活动,表现为膀胱充盈过程中逼尿肌压力的不自主升高,伴随少量漏尿。
(2)心血管自主神经功能评价:卧立位试验或直立倾斜试验可用于评估体位性低血压,直立倾斜试验的倾斜角度规定为60°~80°。诊断体位性低血压时要求患者在卧立位试验/直立倾斜试验中直立3min或10min内(直立不同时间的诊断级别不同,具体见表2,3)收缩压下降≥20 mmHg(1mmHg=0.133 kPa),伴或不伴舒张压下降≥10mmHg,舒张压变化不作为必要条件。由于舒张压下降≥10mmHg诊断体位性低血压特异度较差,因而仅舒张压下降≥10mmHg不能作为体位性低血压的诊断依据。试验期间需排除药物(降压药、抗抑郁药)、低血容量(脱水、急性失血)、心输出量降低(缩窄型心包炎、心肌病、主动脉狭窄)、内分泌疾病(肾上腺功能不全、无功能肾上腺嗜铬细胞瘤)和过度血管舒张(系统性肥大细胞增多症、类癌综合征)等非神经源性因素导致的体位性低血压。鉴别患者是否为nOH,首选卧立位/直立倾斜试验观察患者3min或10min内的心率变化,若心率变化<0.5 搏·min-1·mmHg-1可确诊为nOH,评估期间避免使用影响心率的药物(如β受体阻滞剂等)。Valsalva动作后血压恢复时间延长或血压超射部分消失以及不显著的去甲肾上腺素(NE)水平升高等可进一步支持nOH的诊断(图3)。此外,24h动态血压监测可用于评估MSA患者的夜间高血压。
(3)vPSG:vPSG在RBD的诊断中发挥重要作用,RBD经vPSG证实其异常行为出现于REM睡眠期,且REM睡眠中无肌张力缺失。睡眠呼吸暂停要求口鼻温度传感器或气道正压设备气流或替代呼吸暂停传感器信号曲线峰值较事件前基线值下降≥90%,持续时间≥10 s,睡眠低通气要求鼻压力传感器、气道正压设备气流或替代低通气传感器信号曲线峰值较事件前基线值下降≥30%,持续时间≥10s,且氧饱和度相较于事件前基线下降≥3%,或该事件导致患者觉醒。吸气性叹息在vPSG上表现为鼻压力传感器、口鼻温度传感器和胸腹呼吸感应体积描记绑带的信号曲线峰值较事件前基线升高至少2倍,同时在鼾声通道上可见记录,在视频中可闻及吸气音。为避免呼吸暂停后恢复性深吸气的干扰,呼吸暂停后的吸气性叹息不纳入考虑。
(4)喉镜检查:喘鸣可通过日间临床表现或夜间vPSG记录下的高调吸气声来诊断,纤维喉镜可发现患者声带出现外展障碍或矛盾内收运动,并排除器质性声带病变(如肿块或瘢痕)或非MSA神经源性声带功能障碍。若患者日间喉镜检查正常但临床怀疑喘鸣,则进行药物诱导下睡眠内窥镜检查。
(5)123碘-间碘苄胍-心肌显像(123I-MIBG-scintigraphy):MIBG和NE递质有相似的摄取、储存和释放机制,因而123I-MIBG心肌摄取检查反映节后交感神经突触前末梢功能。心肌123I-MIBG的摄取有2种方式,1种为高浓度时的弥散,发生在早期(注射15~30min后);另一种为低浓度时的延迟摄取(注射3~4h后),反映节后交感神经突触前末梢的摄取能力。MSA患者延迟期心肌/膈肌显像剂摄取比值通常正常,而帕金森病患者的摄取比值下降,提示心肌节后交感纤维功能障碍。影响NE转运和储存的药物、心脏结构性病变、糖尿病导致的末端神经病变也可能导致心肌摄取显像剂减少。
(6)盆底神经生理学:在排除了可能导致慢性神经再生的马尾损伤、盆底手术和产科盆底撕裂的情况下,肛门外括约肌肌电图上若有超过50%的运动单元电位单个持续时间>10ms,或平均持续时间>10ms,则提示患者为MSA-P型,但该表现也可见于PSP和晚期帕金森病患者。6年以上病程的患者若表现出正常的肛门外括约肌肌电图,通常不考虑诊断为MSA。
(7)发汗试验:体温调节汗液试验(TST)可评估患者整体的出汗功能,定量催汗轴突反射试验(QSART)可评估节后交感排汗纤维的功能。TST和QSART的组合可用于判断节前、节后或混合型泌汗功能异常。

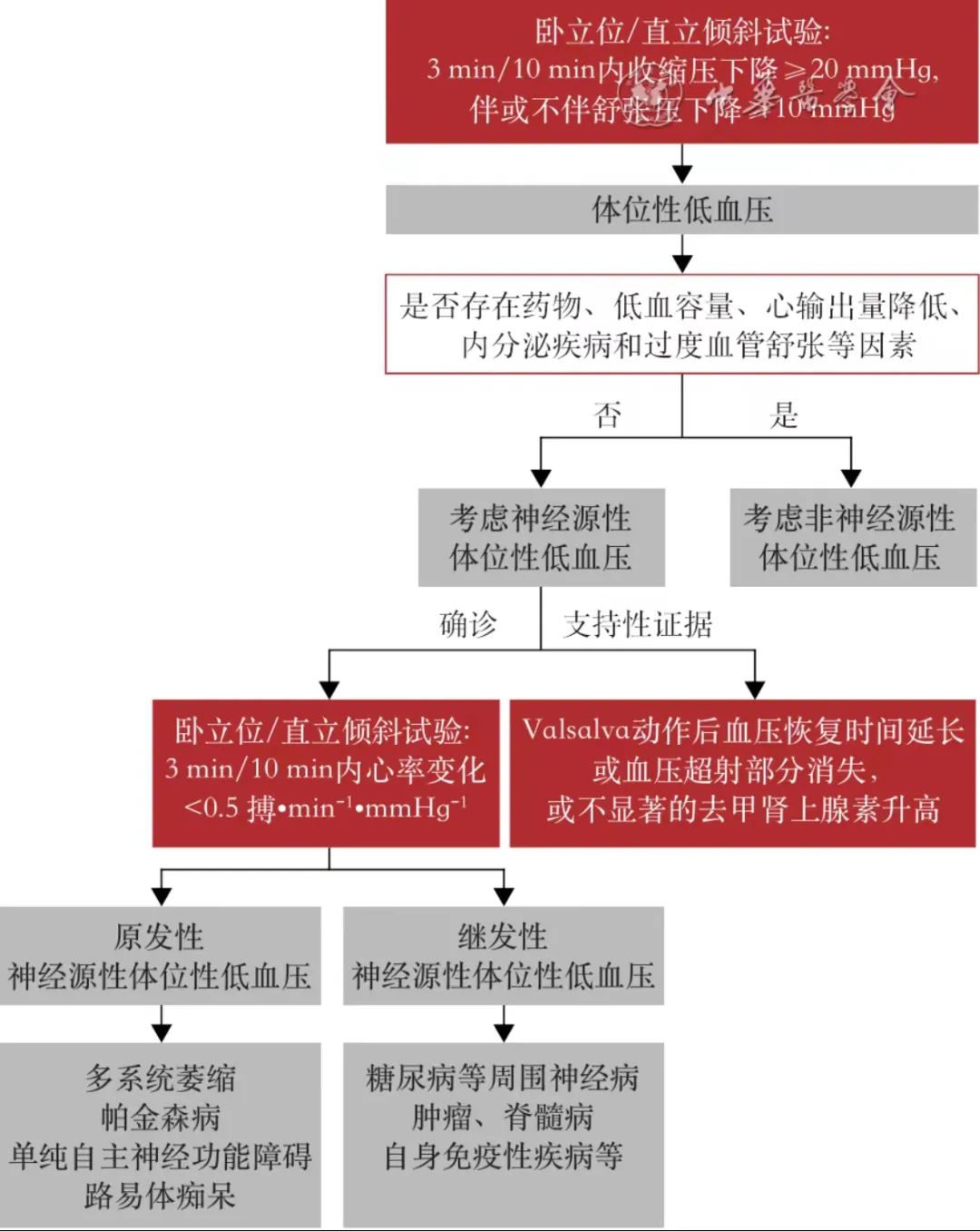
图3 神经源性体位性低血压的诊断流程图
MSA-P型患者可通过判断其对左旋多巴的疗效来辅助诊断,可通过服药史获得相关信息,对于无相关病史的患者或服药效果不明确的患者(图4),可进行急性左旋多巴冲击试验。具体流程如下:要求停用左旋多巴12h,停用单胺氧化酶B抑制剂24h,停用多巴胺受体激动剂72h,并在试验开始前2d口服多潘立酮(20mg,3次/d)以减轻左旋多巴诱导的呕吐和体位性低血压。对于初次就诊未服药的患者,使用200mg/50mg的复方左旋多巴试剂(左旋多巴/外周多巴脱羧酶抑制剂),对于有服药史的患者,使用晨左旋多巴等效剂量的1.5倍,若该剂量仍小于200mg/50mg的复方左旋多巴试剂,则直接服用200mg/50mg的复方左旋多巴试剂,空腹服药。在服药前和服药后30min、1.0h、1.5h和2.0h(或患者自身感觉运动功能恢复最佳的时候)分别评定修订版运动障碍协会统一帕金森病评定量表Ⅲ(MDS- UPDRSⅢ)评分,若评分改善
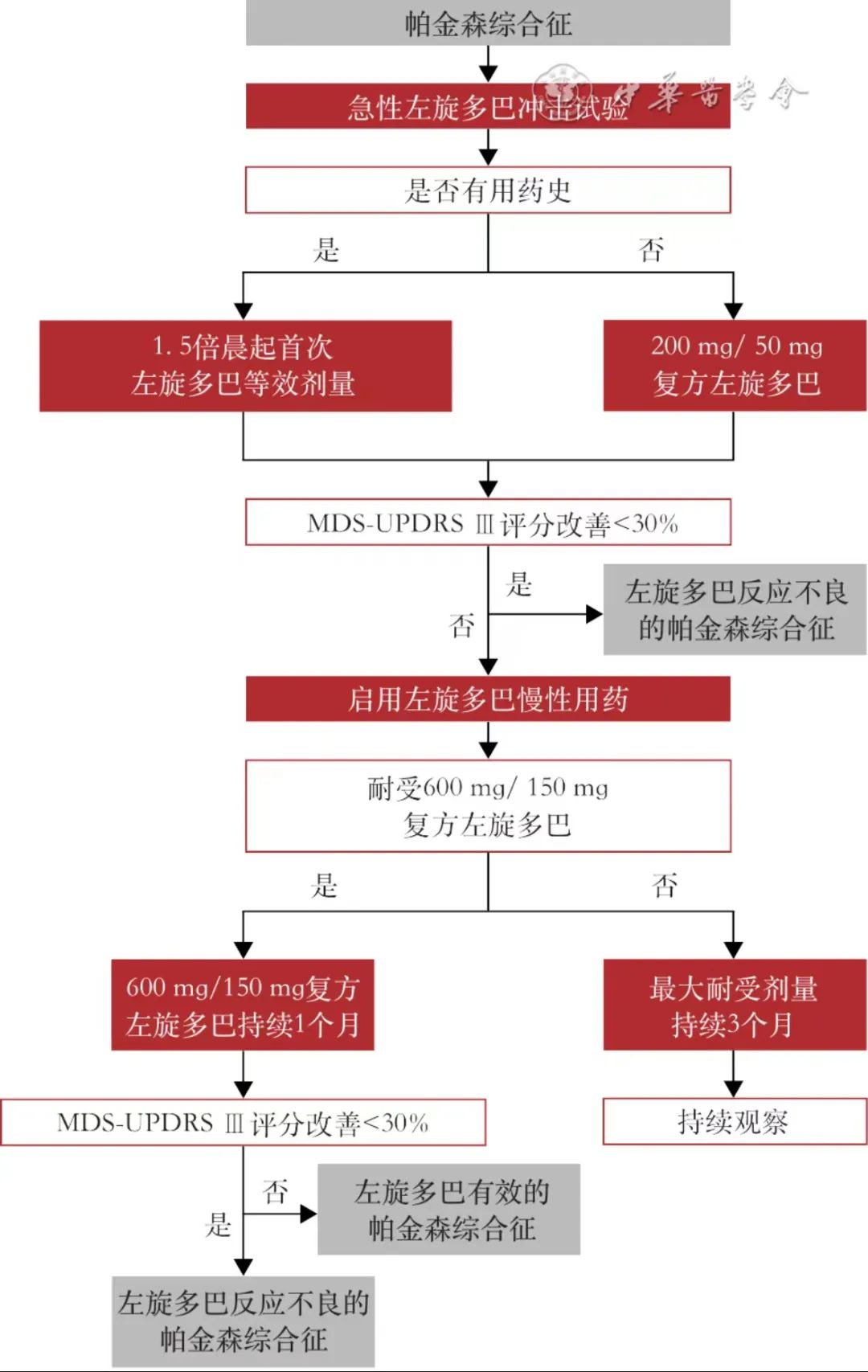
图4 左旋多巴反应不良的帕金森综合征诊断流程图
4.生化检查
(1)仰卧位血浆NE水平:测量前需停用咖啡因、酒精、尼古丁12h,停用对乙酰氨基酚5d,测量血浆左旋多巴含量
(2)蛋白质错误折叠循环扩增(PMCA)/实时震动诱导转换(RT-QuIC):利用PMCA技术扩增脑脊液中的α-突触核蛋白寡聚体后,通过硫黄素T荧光来反映扩增后的纤维含量。MSA患者脑脊液中的α-突触核蛋白扩增后硫黄素T荧光值低于2000,而帕金森病和DLB患者的硫黄素T荧光值明显升高,可用于鉴别MSA与帕金森病、DLB。
(3)脑脊液中的神经纤维轻链(NfL):酶联免疫吸附试验检测脑脊液中的NfL水平>1400pg/ml提示患者为MSA,帕金森病和DLB患者的NfL水平较低,若PAF患者脑脊液NfL水平>1400pg/ml,则提示PAF会向MSA转变。
(4)皮肤活组织检查(活检)免疫组织化学试验:MSA患者中α-突触核蛋白通常沉积于体神经纤维末端,帕金森病患者的α-突触核蛋白通常沉积于自主神经纤维末端,因此对皮肤小动脉、汗腺、立毛肌等自主神经调控的组织进行活检可发现,MSA患者无明显的α-突触核蛋白沉积,帕金森病患者则有显著的α-突触核蛋白沉积。
5.基因检测
MSA无明确致病基因。为鉴别遗传性共济失调与MSA-C型患者,可筛查共济蛋白基因(FXN)、突触核膜蛋白基因(SYNE 1)、Aprataxin基因(APTX)、Senataxin基因(SETX)、ATXN1、ATXN2、ATXN3、ATXN7、钙离子电压门控通道亚单位α1A基因(CACNA1A)、TATA结合蛋白基因(TBP)、脆性X信使核糖核蛋白1基因(FMR1)等。
欧洲多系统萎缩研究组于2004年建立了统一多系统萎缩评价量表(UMSARS),UMSARS包括病史回顾、运动检查、自主神经功能检查和整体失能程度4个项目,评分越高提示症状越重,是评估MSA病情进展首选的半定量评估量表。但随着UMSARS的广泛应用,其局限性也逐渐显露:(1)UMSARS中部分项目能较好地反映疾病进展,尤其是与运动功能评估相关的项目,而与自主神经功能评估相关的项目对疾病进展不敏感。(2)UMSARS评估在疾病晚期存在天花板效应,不能有效反映晚期疾病进展。(3)UMSARS对部分MSA相关的症状缺乏评估,如喘鸣、睡眠障碍、流涎、发声障碍、挛缩疼痛等。(4)UMSARSⅢ要求记录站立2 min后的血压和心率,但MSA诊断标准评估的是站立/直立倾斜试验3min内的变化。这提示我们MSA患者的评估还有赖更加全面和准确的评估量表。
其他运动功能评定量表:MDS-UPDRS于2008年由UPDRS扩增修改而来,分为4个部分,包括日常生活中的非运动表现、运动表现、运动评估和运动并发症,MSA患者常用MDS-UPDRS来评估运动改善情况。MSA患者还可利用Tinetti步态和平衡测试、Berg平衡量表、步态及摔倒问卷、改良Webster量表来评估运动功能。
非运动功能评定量表:非运动症状筛查量表、帕金森病结局量表-自主神经系统功能障碍、嗅棒试验16、Wexner便秘评分、快速眼球运动期睡眠行为障碍筛查量表、匹兹堡睡眠质量指数、帕金森病睡眠质量量表、39项帕金森病调查问卷可用于评估患者的非运动功能和生活质量,利用汉密尔顿抑郁量表、汉密尔顿焦虑量表、蒙特利尔认知评估、简易精神状态检查量表、额叶功能评分等评估患者的精神心理状态。
此外,利用嗓音障碍指数、吞咽筛查量表、标准吞咽功能评价量表评估患者的咽喉功能。
目前MSA的诊断主要参考2022年MDS提出的诊断标准和2017版多系统萎缩诊断标准中国专家共识,结合我国MSA的相关临床研究,将MSA根据诊断精确度分为神经病理确诊的、临床确诊的、临床很可能的和前驱可能的MSA。
1.神经病理确诊的MSA:相当于之前诊断标准中确诊的MSA,尸检病理结果显示中枢神经系统大量胶质细胞胞质内含有α-突触核蛋白阳性的包涵体,并存在纹状体黑质或橄榄桥脑小脑结构的神经退行性改变。
2.临床确诊的MSA:需要满足散发、进展性、成年起病(>30岁)的基本特征,同时具有核心临床表现,至少存在2项支持性临床表现,至少存在1项MRI标志,不存在排除性的临床表现(表2)。
3.临床很可能的MSA:需要满足散发、进展性、成年起病(>30岁)的基本特征,同时具有核心临床表现,至少存在1项支持性临床表现,不要求MRI标志,不存在排除性的临床表现(表2)。
4.前驱可能的MSA:需要满足散发、进展性、成年起病(>30岁)的基本特征,必须具有至少1项临床非运动特征(准入标准),同时具有至少1项临床运动特征,不存在排除性临床表现(表3)。
1.帕金森病:帕金森病患者的帕金森综合征对多巴胺能药物的疗效明确且显著有效,常伴静止性震颤与嗅觉减退。MSA-P型患者对左旋多巴疗效欠佳,可伴有姿势性与动作性震颤,嗅觉减退少见,可早期出现进展性的严重自主神经功能障碍。借助MRI、18F-FDG-PET、D2受体成像、经颅超声成像、123I-MIBG-心肌显像进行鉴别。
2.PSP:PSP患者通常表现出垂直核上性凝视麻痹或垂直扫视变慢,较MSA更早出现反复的自发性摔倒与冻结步态,可伴有左旋多巴反应不良的帕金森综合征和认知障碍,通常无nOH。MSA-P型患者可表现出小脑性眼球运动障碍,姿势平衡障碍较PSP进展稍慢,认知障碍少见,而伴有显著的自主神经功能障碍显著,可出现RBD。两者可借助神经影像学检查进行鉴别。
3.DLB:痴呆是DLB患者的必要特征,可表现为早期注意力、执行功能和视觉空间能力的损害,在注意力与警觉方面呈波动性认知障碍,有反复发作的视幻觉,可伴有左旋多巴反应不良性帕金森综合征和RBD。MSA-P型患者多不伴有痴呆、波动性认知障碍与视幻觉,可早期出现进展性的严重自主神经功能障碍。两者可借助结构MRI和分子显像进行鉴别。
4.CBS:CBS患者常出现不对称的四肢肌强直或运动不能、肌张力障碍和肌阵挛,同时可出现口颊或肢体失用、皮质复合感觉丧失和异己肢体。MSA-P型患者四肢肌强直多对称,且少见口颊或肢体失用、皮质复合感觉丧失以及异己肢体等,两者可借助结构MRI和分子显像进行鉴别。
5.SAOA:SAOA主要指成年发病的、没有明确家族史的进展性共济失调患者,现病因未明,患者疾病进展相对较慢,不出现严重的自主神经功能障碍。MSA-C型患者可早期出现进展性的自主神经功能障碍,借助MRI、DAT-SPECT进行鉴别。
6.脆性X相关震颤/共济失调综合征(FXTAS):FXTAS多在50岁以后发病,为X连锁遗传,男性多见,以意向性震颤、小脑性共济失调步态、帕金森综合征候群、认知功能减退、周围神经病及自主神经功能障碍为主要临床表现。头颅MRI可见小脑中脚白质病变。基因检测可发现FMR1基因突变。MSA-C型患者认知障碍少见。
7.脊髓小脑性共济失调(SCA):SCA是一组由基因突变导致的小脑、脑干、脊髓退行性变,以进行性小脑性共济失调、构音障碍为主要临床表现,可伴有锥体外系症状、锥体束症状、认知障碍、视力障碍、肌阵挛、眼肌麻痹等其他神经系统体征的遗传性疾病。患者可有家族史,不出现严重的自主神经功能障碍。影像上SCA患者与MSA-C患者有重叠,通过基因筛查明确诊断。
类型:原创
病例ID:ZYLM000003868
校对:王宇军
阅读:2763
文章已于2023-12-16修改






