患者:女,52岁。
主诉:头晕三天。
现病史:患者三天前无明显诱因出现头晕,偏头时明显,无明显头痛,无发热,有恶心呕吐,无意识障碍,无肢体抽搐、乏力,无大小便失禁。至当地医院就诊,行颅脑CT检查示左侧额叶肿瘤性病变并出血。为求进一步诊治,逐至**市中心医院就诊,门诊以“脑内出血”收入院。入院以来,患者神清,精神食欲睡眠差,大小便正常。
病案讨论
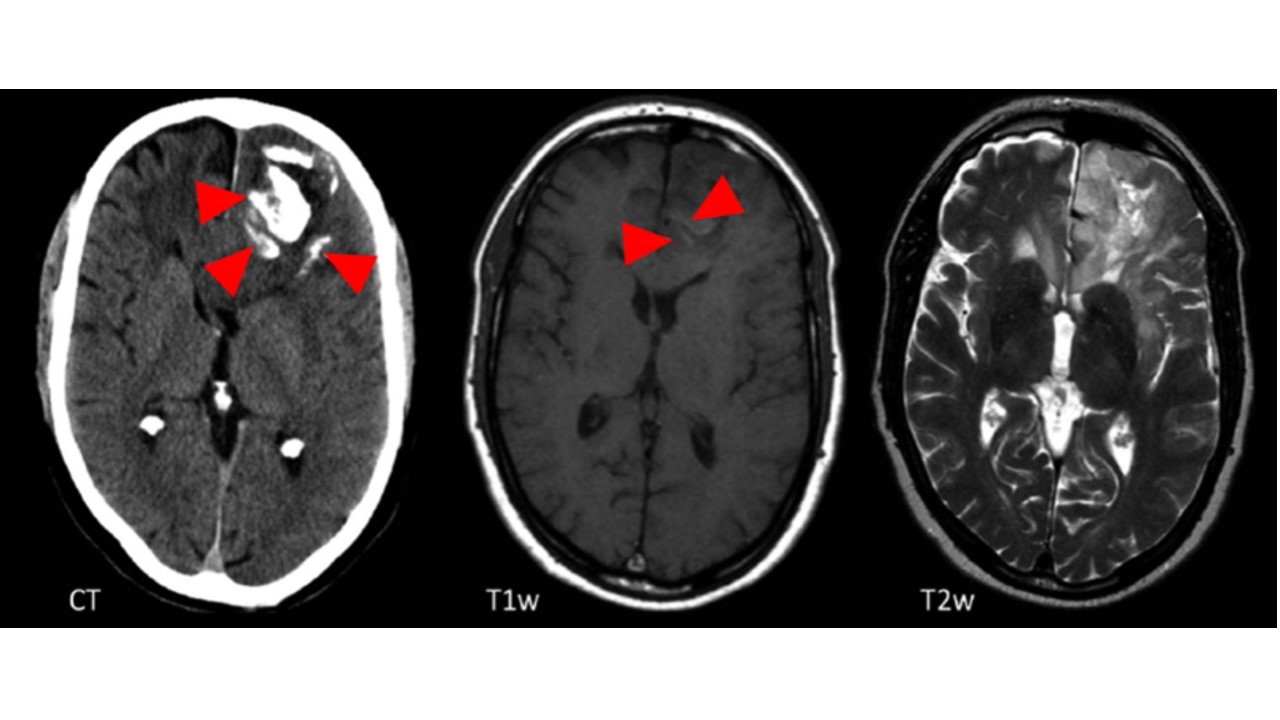
MR平扫及增强示:左侧额叶见不规则片状稍长T1、T2信号为主异常信号,其内可见不规则短T1、T2信号,病灶边界不清,DWI显示局部扩散受限,增强后病灶轻度不均匀强化。
颅脑CTA:可见病灶内见条片状、树枝状钙化灶。
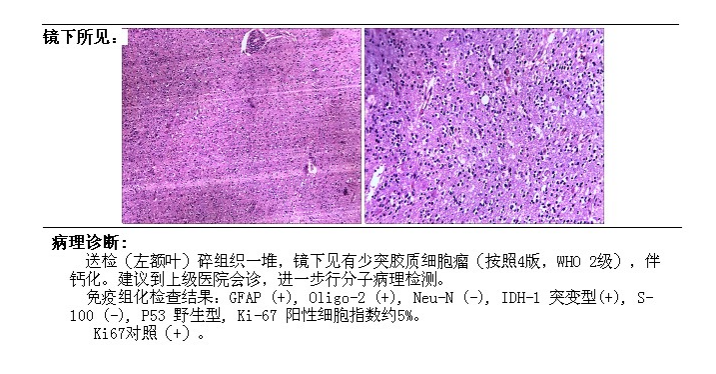
免疫组化:GFAP(+),Oliga-2(+),Neu-N(-),IDH-1突变型(+),S-100(—),P53野生型,Ki-67阳性细胞指数约5%。
病理诊断:送检(左额叶)碎组织一堆,镜下见有少突胶质细胞,伴钙化。最终诊断为少突胶质细胞瘤(WHO 2级 NOS)。
少突胶质细胞肿瘤(oligodendrogliomas, OGS)是成人常见的胶质瘤之一,占原发性颅内肿瘤的5%~10%,患病率仅次于星形细胞瘤。肿瘤具有弥漫浸润生长特点,影像表现多样,术前诊断和鉴别存在困难。近年来,有关OGS的较多研究表明,肿瘤的分级、分型与患者对化疗药物的敏感性和预后密切相关,因此术前评估OGS级别意义重大。
OGS起源于神经上皮组织,是成熟少突胶质细胞或未成熟的神经胶质前体细胞的肿瘤转化。WHO将OGS分为2级少突胶质细胞瘤(oligodendroglioma, OD)和3级间变型少突胶质细胞瘤(anaplastic oligodendroglioma, AO)。需要特别提出的是,3级AO为原发或由3级OD进展而来。
WHO 2级OD好发于40~50岁成年人,WHO 3级AO平均发病年龄较OD更大,幕上额叶皮层或皮层下白质区是其好发部位。
临床表现为头痛、癫痫和局部神经功能缺损。
治疗 该肿瘤的治疗以手术切除为主,术后应辅以放、化疗。该类肿瘤的预后与分级有关,也与分子分型相关。新版WHO分型将OGS增加了分子分型,分为异柠檬酸脱氢酶(isocitrate dehydrogenase, IDH)突变和1p/19q共缺失型和非特指类型(NOS),本例未做分子检测,为NOS。伴1p/19q共缺失和IDH1突变分型肿瘤较非特殊类型预后好,放疗效果更显著。
肿瘤大体标本:OD和AO均为实性,位于皮层或皮层下白质区的浸润性肿块。肿瘤界限较清楚,质软,呈灰粉色,无包膜,易钙化,AO较OD囊性变和出血更多见。
镜下改变:OD瘤细胞密度中等,细胞核圆居中,大小一致,比正常少突胶质细胞稍大,胞质透亮,呈典型的煎蛋样或蜂窝状特征,核周有空晕,核分裂象少或无。血管结构显示典型的分支状毛细血管网。细胞增值指数小于5%;AO瘤细胞密度高,异型性明显,核分裂象多,微血管增生,伴或不伴假栅栏样结构的坏死。肿瘤细胞核圆深染,核周有空晕,局灶性微钙化常见,血管结构以微血管增生为主,也可见分支状毛细血管。
免疫组织化学:少突胶质细胞转录因子2(Olig-2)是OGS特异性的免疫组织化学标志物。胶质纤维酸性蛋白(glial fibrillary acidic protein, GFAP)、酸性钙结合蛋白(S-100 protein)通常也有表达。
分子病理:依据新版WHO诊断标准对OGS进行分子分型。50%~70%2级病例伴1p/19q缺失和IDH1突变;30%~40%3级病例伴1p/19缺失;儿科病例中,2级肿瘤经常伴IDH阴性和O-6-甲基鸟嘌呤-DNA甲基转移酶(MGMT)阳性,X连锁α-地中海贫血/精神发育迟缓综合征基因(ATRX)为野生型。
影像表现:WHOI2级OD好发于皮层或皮层下白质区,幕上额叶最常见,其次是颞叶,也可发生于顶叶或枕叶,团块状肿物。CT表现为混杂密度(等/低密度),常有结节状、团块状或脑回样钙化,瘤内囊变多见,出血和瘤周水肿少见,可见肿瘤邻近颅骨扩大、侵蚀。MRI表现病灶边界清楚,信号不均匀,T1WI常呈低、等信号,T2WI呈不均匀高信号,信号不均匀是由于钙化、囊变所致。T2-FLAIR序列呈不均匀高信号,DWI显示扩散不受限或轻度受限。GRE或SWI可显示瘤内钙化,但MRI对钙化的显示不及CT。强化方式呈无强化或轻度强化,罕见柔脑膜强化。MRS表现为Cho峰增高、NAA峰减低,缺乏Lip/Lac峰,有助于与AO鉴别。 PWI提示相对脑血容量(rCBV)增高。WHO 3级AO好发位置及肿瘤CT表现与OD相似。常有结节状、团块状或脑回样钙化,瘤内囊变多见,出血、水肿、坏死较Ⅱ级多见,邻近颅骨可扩大、重塑、侵蚀。MRI表现为病灶边界不清楚,信号不均匀,T1WI呈不均匀低信号,T2WI呈不均匀高信号,FLAIR序列呈不均匀高信号,DWI扩散不受限或轻度受限。增强扫描强化方式多变,AO较低级别OD强化更多见,环状强化少见,若出现常提示预后不良。由于肿瘤呈弥漫浸润,可在异常信号区外发现肿瘤细胞。MRS表现为Cho/Cr升高,NAA峰减低,1.33 ppm可见Lip/Lac峰。PWI表现为rCBV明显增高,能帮助鉴别2级与3级少突胶质细胞瘤和引导活检。
鉴别诊断:(1)胶质母细胞瘤:胶质母细胞瘤属于WHO Ⅳ级肿瘤,恶性程度相对较高,发病年龄相对较大,发病部位较深,信号不均匀,95%有坏死核心,出血多见,增强呈明显花环样强化,多有子灶。(2)弥漫性星形细胞瘤 IDH突变型。(3)单发转移瘤:发病年龄较大,有原发肿瘤病史,常位于灰、白质交界区,瘤周水肿明显;MR功能成像有助于两者的鉴别。转移瘤强化边缘区NAA/Cho比值接近正常脑组织波谱,而AO则明显降低;转移瘤ADC值高于AO,DWI扩散受限不显著。
参考文献:中华放射学杂志2020,54(6):621-624
类型:原创
病例ID:ZYLM000003137
校对:王宇军
阅读:1087
文章已于2023-09-24修改






